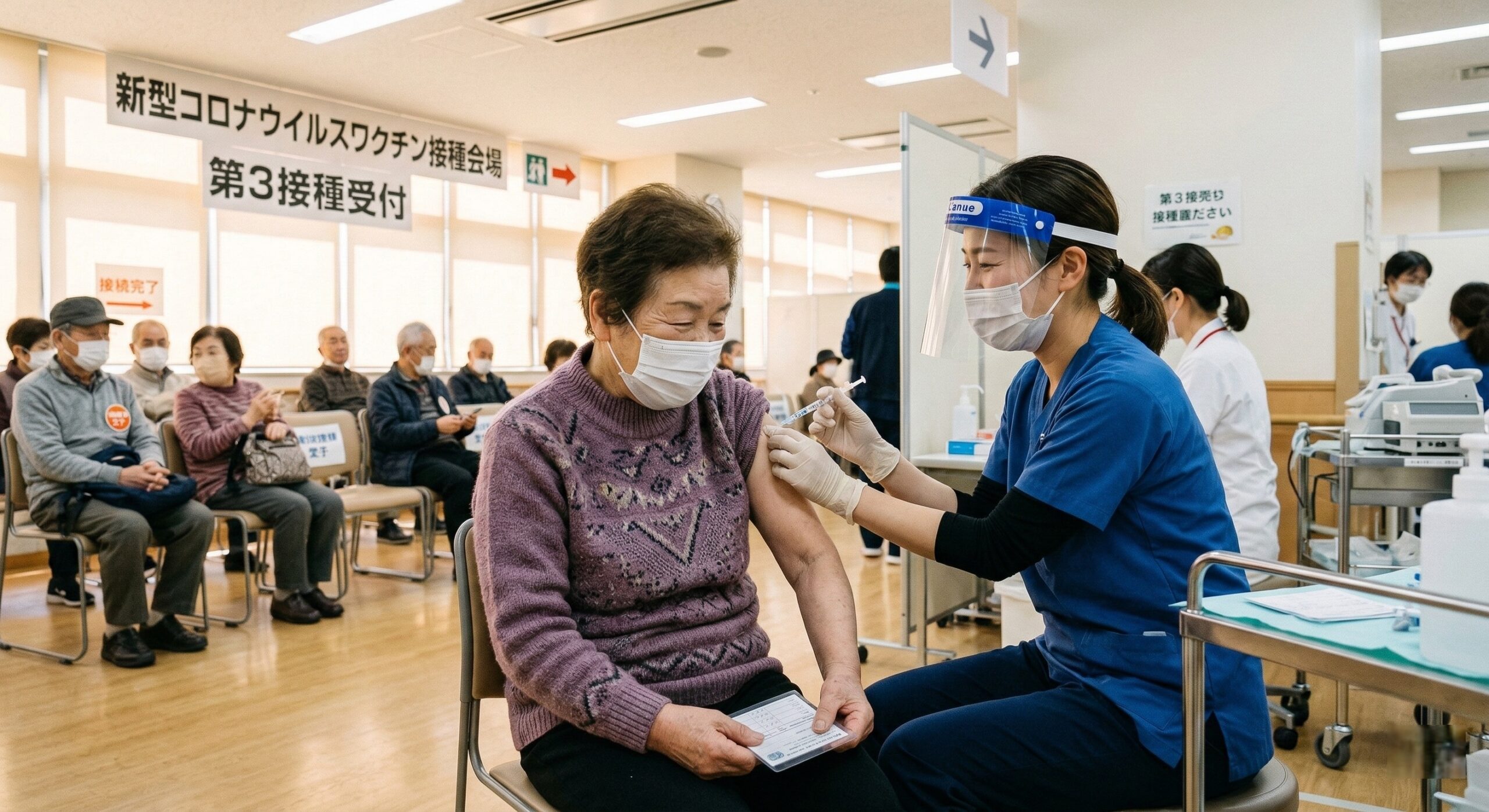
「ワクチン治験」と一言で言っても、その種類や背景にある科学、そして国の戦略は多岐にわたります。あなたの身体を『価値ある資本』と捉え、効率的な治験参加を目指すあなたにとって、日本のワクチン開発の全体像を理解することは、未来の案件選定における重要な判断材料となるでしょう。
過去から現在へ:日本のワクチン政策が辿った道のり
日本のワクチン政策は、第二次世界大戦後の公衆衛生の再建期から現代に至るまで、感染症の脅威、科学技術の進展、そして法制度と社会的情勢の相互作用によって幾度もの変遷を遂げてきました。この歴史的変遷を理解することは、現在のワクチン治験の背景を深く知る上で不可欠です。
1948年体制と「義務的集団接種」の時代
1948年に制定された旧予防接種法は、戦後の混乱期における天然痘やポリオといった急性伝染病の蔓延を抑止することを主眼に置いていました。この時代、国民には予防接種を受ける「義務」が課されており、学校などでの「集団接種」が一般的でした。社会全体の流行を抑える「集団免疫」の考え方が国家レベルで具現化されていたのです。
しかし、1970年代から80年代にかけて、ワクチンの副反応や効果の個人差が社会的に問題視され、接種後の健康被害を巡る訴訟が相次ぎました。
1994年改正:公衆衛生から個人の医療判断への転換
日本のワクチン政策における最大の転換点は、1994年(平成6年)の予防接種法改正です。これは、1980年代後半からの予防接種訴訟における国の敗訴や、MMR(麻疹・おたふくかぜ・風疹)混合ワクチンの副反応問題が背景にありました。
この法改正では、以下の三つの大きな変更がなされました。
- 「義務」から「努力(勧奨)」へ: 法的義務が廃止され、国民に接種を受けるよう努めることを求める「努力義務(勧奨)」規定へと緩和されました。
- 「集団」から「個別」へ: 学校等での一斉接種が廃止され、個々の医療機関において医師の診断に基づき接種を受ける「個別接種」へと移行しました。
- 対象疾患の除外: インフルエンザは、当時の社会的認識として「副反応のリスクが効果を上回る可能性がある」と判断され、定期接種の対象から一度除外されました。
この改正は、ワクチンを「国家が国民に強制する公衆衛生の道具」から、「個人の健康管理における選択肢」へと再定義したことを意味します。
現代の予防接種制度:定期接種と任意接種
1994年の改正を経て、日本の予防接種制度は現在の「定期接種」と「任意接種」の二層構造として定着しています。この区分は、法的根拠、費用負担、そして副反応発生時の救済制度において明確に異なる設計がなされています。
| 項目 | 定期接種 | 任意接種 |
|---|---|---|
| 法的根拠 | 予防接種法 | なし(薬機法による承認のみ) |
| 実施主体 | 市区町村(公費負担) | 個人と医療機関の契約(自己負担) |
| 対象疾患の例 | BCG、MR、DPT-IPV、B型肝炎等 | おたふくかぜ、インフルエンザ等 |
| 対象年齢 | 法律で定められた期間内 | 制限なし(希望時) |
| 健康被害救済 | 予防接種健康被害救済制度(高額補償) | 医薬品副作用被害救済制度(PMDA) |
定期接種による健康被害が生じた場合は、厚生労働大臣が認定する「予防接種健康被害救済制度」が適用され、手厚い補償が受けられます。一方、任意接種の場合は、独立行政法人医薬品医療機器総合機構(PMDA)が運営する「医薬品副作用被害救済制度」が適用されます。
パンデミックが加速させた技術革新:新モダリティワクチンの台頭
2020年以降の新型コロナウイルス感染症の世界的流行は、世界のワクチン開発の歴史における特異点となりました。これまでの弱毒化や不活化といった伝統的ワクチンから、遺伝情報を利用した「新モダリティ」への移行が急速に進んだのです。
mRNAワクチンの仕組みと開発の歴史
mRNAワクチンは、病原体そのものやそのタンパク質を直接注入するのではなく、標的となるタンパク質(例えばウイルスのスパイクタンパク質)の「設計図」であるメッセンジャーRNA(mRNA)を脂質ナノ粒子という微細なカプセルに封入して体内に導入する技術です。
この技術の根幹となる、外来性mRNAが生体内で翻訳・発現されるという考え方は1990年には既に実証されていました。mRNAワクチンの利点は、病原体の培養が不要であるため、遺伝子配列さえ特定できれば極めて短期間で製造ラインを立ち上げられる点にあります。
ウイルスベクターと組み換えタンパク技術
mRNAワクチンと並んで実用化されたのが「ウイルスベクターワクチン」です。これは、無害化した別のウイルス(アデノウイルス等)を運び役として、標的となる病原体の遺伝子を細胞内に届ける手法です。
また、「組み換えタンパクワクチン」は、遺伝子組み換え技術を用いて体外(昆虫細胞など)で抗原タンパク質を製造し、それを精製して接種する手法です。
次世代の旗手:レプリコンワクチン
最近、日本において世界で初めて製造販売承認を取得したのが「レプリコンワクチン(自己増殖型mRNAワクチン)」です。これは、細胞内に入ったmRNAが自らを複製(増殖)する酵素の情報を併せ持つもので、従来のmRNAワクチンと比較して、極めて少量の投与量で高い免疫効果を維持できるという特性があります。
レプリコン技術には、以下の三つの大きなメリットが期待されています。
- 低用量・高効率: 投与量が少なくて済むため、発熱や倦怠感などの初期の副反応を抑えられる可能性があります。
- 免疫の持続性: 抗原が体内で一定期間増殖し続けるため、免疫応答が長期間持続し、追加接種の頻度を減らせる可能性があります。
- 迅速な大量生産: 1人あたりの必要量が少ないため、同じ製造規模でより多くの人数分のワクチンを短期間に生産できます。
一方で、この技術は「自己増殖」という性質から、体内での制御や他者への伝播に関する懸念がインターネット等で拡散されていますが、現在認可されているワクチンについては、厳格な治験データに基づき安全性が確認されています。
国家戦略SCARDA:日本のワクチン自給と国際貢献への挑戦

パンデミック時に海外製ワクチンの導入に依存せざるを得なかった経験を受け、日本政府は2021年6月に「ワクチン開発・生産体制強化戦略」を閣議決定しました。これは、ワクチン開発を公衆衛生のみならず、経済安全保障および外交の柱として位置づける抜本的な国家戦略です。
SCARDAの設立と司令塔機能の強化
この戦略の目玉として、2022年3月に国立研究開発法人日本医療研究開発機構(AMED)内に「先進的研究開発戦略センター(SCARDA)」が設置されました。SCARDAは、平時から感染症有事を見据えた戦略的な研究費の配分を行い、基礎研究から治験、実用化までを一気通貫でマネジメントする「司令塔」として機能します。
SCARDAの主な役割は以下の通りです。
- 戦略的ファンディング: 内閣官房予算約1,500億円等を活用し、有望なモダリティやワクチンシーズに対して機動的に資金を提供します。
- 情報収集・分析: 国内外の技術動向、知財情報、感染症の発生動向を分析し、開発戦略を常に更新します。
- 国際連携: 感染症流行対策イノベーション連合等の国際機関と連携し、グローバルな開発枠組みに日本が深く関与する体制を構築します。
SCARDAは、日本全国の大学の知を統合するため、東京大学を「フラッグシップ拠点」とし、特定の強みを持つ4つの大学を「シナジー拠点」として整備しました。
製造基盤の整備:デュアルユース設備の導入
開発能力の強化と並行して進められているのが、国内での「大規模製造能力」の確保です。経済産業省主導のもと、「ワクチン生産体制強化のためのバイオ医薬品製造拠点等整備事業」が進められており、平時にも有事にも稼働できる「デュアルユース(二重用途)」設備の整備に多額の予算が投じられています。
デュアルユース設備の戦略的意義は、平時には抗体医薬品などのバイオ医薬品を商業生産し、感染症有事には国の指示によって短期間でパンデミックワクチン製造へ切り替える仕組みにあります。
現在、国内の主要事業者として第一三共、Meiji Seika ファルマ、塩野義製薬、KMバイオロジクス、武田薬品工業、JCRファーマなどが採択され、整備が進んでいます。これらの整備により、政府が掲げる「100日以内に国民全員分のワクチンを供給する」という目標の達成に向けたインフラが整いつつあります。
重点感染症の選定と研究開発ターゲット
SCARDAおよび厚生労働省は、限られた資源を集中させるため、公衆衛生および安全保障上の重要度に基づいて「重点感染症」を定義しています。
- グループA (新感染症): 未知のインフルエンザ、コロナウイルス、出血熱ウイルスなど。
- グループB (既知の脅威): MERS、SARS、RSウイルス、デング熱、エボラ出血熱など。
- グループC (薬剤耐性菌): 薬剤耐性結核、多剤耐性緑膿菌など。
- グループD (希少・生物毒): マラリア、狂犬病、ヘビ毒など。
この優先順位に基づき、各研究拠点と産業界が連携し、臨床試験の枠組みをあらかじめ策定しておくことで、有事の際のタイムラグを最小限に抑える試みがなされています。
未来を拓く治験:現在進行中の主要ワクチン開発動向
現在、日本国内では新型コロナウイルスに対する次世代ワクチンの改良のみならず、これまで実用化が困難であった疾患や、がんなどの非感染性疾患に対する「治療用ワクチン」の治験が活発に行われています。治験参加が、これらの最先端医療の発展に貢献する「投資」としての側面を持つことは言うまでもありません。
次世代新型コロナ・感染症ワクチン
新型コロナウイルスについては、流行株の変化に合わせた迅速なアップデートが治験の中心となっています。
- レプリコンワクチンの多角化: VLP Therapeutics Japanなどにより、新型コロナ変異株に対するレプリコンワクチンの開発が進んでおり、既存のmRNAワクチンよりも長期間の免疫維持を目指した治験が行われています。同社はインフルエンザ、デング熱、マラリア等に対してもレプリコン技術の応用を計画しています。
- 粘膜ワクチン: 注射型では誘導が難しい「粘膜免疫」を鼻腔や経口で惹起するワクチンの開発が、初期臨床試験に向けて準備されています。これは感染そのものを阻止する能力の向上を目的としています。
- RSウイルスワクチン: 高齢者および妊婦を対象としたRSウイルスワクチンの治験が進んでおり、国内企業による次世代型の開発も進行中です。
個別化がんワクチンのブレイクスルー
近年、最も注目されている分野の一つが「がんワクチン」です。これは予防ではなく、患者のがん細胞を攻撃する免疫系を強化する治療を目的としています。
- NECグループ(NECVAX-NEO1): 最先端のAI技術を用いて、患者個人のがん細胞に存在する特有の変異「ネオアンチゲン」を予測し、それを標的とするワクチンを設計します。固形がん患者を対象とした第I相臨床試験において、安全性と高い免疫原性が確認され、良好な概念実証が得られたことが2025年12月に発表されました。
- ブライトパス・バイオ(BP2301/BP2202): 固形がんを標的とした「自家CAR-T細胞療法」や、iPS細胞から作製する「他家CAR-NKT細胞療法」の治験が進行中です。
- オンコセラピー・サイエンス: 複数の固形がんに対するペプチドワクチンの治験を継続しており、チェックポイント阻害剤との併用による相乗効果の検証が進められています。
希少・輸入感染症への挑戦
SCARDAの支援により、市場性が低いためにこれまで開発が放置されていた感染症への対策も動き出しています。
- デング熱・出血熱ワクチン: 長崎大学などでは、熱帯地域で甚大な被害をもたらしているデング熱に対し、mRNAプラットフォームを用いたワクチンの臨床開発が計画されています。
- 薬剤耐性結核ワクチン: 薬剤耐性問題への対策として、新規のアジュバント技術を用いたワクチンの基礎研究から治験への移行が進められています。
治験参加で未来に投資する:賢い選択のための情報活用術
日本のワクチン開発は、過去の教訓を乗り越え、国家戦略として新たなフェーズに入っています。このダイナミックな変化の最前線で、あなたの健康と時間を未来の医療への「投資」として活用することは、社会貢献と自己成長を両立させる賢明な選択となるでしょう。
治験参加は「社会貢献」と「自己投資」の両面を持ちます。最新のワクチン開発動向や国の戦略を理解することは、あなたの「治験ポートフォリオ」を最適化するための重要な判断材料となります。治験に参加する際は、PMDAの公式サイトなど、信頼できる情報源で治験情報を確認してください。
今日ご紹介したような、最先端の医療技術に貢献する治験情報。私たちは、あなたの「時間を、価値に変える。未来を、健康でつなぐ。」ための正確で価値ある情報を提供し続けています。もし、あなたも未来の医療に貢献しながら自己投資をしたいと考えているなら、治験ネットがその一助となるでしょう。
治験ネットについて
「時間を、価値に変える。未来を、健康でつなぐ。」
治験ネットは、治験への参加を「時間の投資」と捉え、納得できる情報提供を大切にしています。ワクチン・生活習慣病・美容など幅広い分野の募集情報を掲載中。会員登録(無料)で、あなたの条件に合った案件を確認できます。
→ 会員登録ページへ
参考・出典
- 予防接種各論 – インフルエンザウイルスワクチン – kusakari-shounika.or.jp(日本のインフルエンザワクチンに関する歴史的背景や制度の変遷について解説されています。) https://www.kusakari-shounika.or.jp/library/57b57ffcd8f117112ca60ac2/57ff0b4a63c0262433e504d1.pdf
- 日本におけるインフルエンザワクチンの歴史 | コラム | 診療予約システム・WEB問診|テルミーアイ(日本のインフルエンザワクチン政策の歴史的経緯と集団接種から個別接種への移行について記述されています。) https://www.aiakos.co.jp/column/history-vcflu-japan/
- 過去・現在・未来で読み解く,日本の予防接種制度(齋藤昭彦 … – igaku-shoin.co.jp(日本の予防接種制度の歴史、特に1994年の法改正とその背景にあるMMRワクチン問題について詳細に解説されています。) https://www.igaku-shoin.co.jp/paper/archive/y2014/PA03058_02
- 医療機関の公開情報(定期予防接種の定義、対象疾患、対象年齢について解説されています。) https://www.hiro-clinic.or.jp/pediatrics/column/routine-vaccination-guide/
- 定期接種と任意接種の違い – cocoromi-cl.jp(定期接種と任意接種の法的根拠、費用負担、対象疾患の違いについて説明されています。) https://cocoromi-cl.jp/knowledge/pediatric-medicine/childrens-vaccinations/regular-and-optional/
- A- 定期接種と任意接種のワクチン – 日本小児科学会(定期接種と任意接種の制度的区分、対象疾患の例、健康被害救済制度の概要が示されています。) https://www.jpeds.or.jp/uploads/files/VIS_A-02teikiseishu_20240401.pdf
- 定期接種と任意接種 – ワクチン.net(定期接種と任意接種の違い、健康被害救済制度の二面性について説明されています。) https://www.wakuchin.net/about/universal.html
- 新型コロナウイルスワクチンの国内導入にあたって―mRNAワクチンとウイルスベクターワクチンの基本 – 国立感染症研究所(mRNAワクチンのメカニズム、開発の歴史、迅速な製造を可能にした技術について解説されています。) https://id-info.jihs.go.jp/niid/ja/typhi-m/iasr-reference/10182-492r06.html
- 【動画あり】次世代mRNAワクチン(レプリコン)の製造販売承認を世界で初めて取得。新型コロナウイルス感染症予防に向け供給へ|INSIGHT INSIDE – Meiji Seika ファルマ(レプリコンワクチンの世界初の承認、そのメカニズム、低用量・高効率・持続性といったメリットについて解説されています。) https://www.meiji-seika-pharma.co.jp/insight-inside/8.html
- 【ニュースリリース】新型コロナウイルス変異株レプリコン(次世代mRNA)ワクチン追加接種治験で5mC修飾により低用量・高免疫原性・良好な安全性を確認[iScience論文] – VLP セラピューティクス・ジャパン(レプリコンワクチンの多角化と、新型コロナ変異株に対する開発動向について言及されています。) https://vlptherapeutics.co.jp/press/94704/
- レプリコンワクチンについて【仕組み・お断り・治験】 | ひまわり医院(内科・皮膚科)(レプリコン技術の「自己増殖」に関する懸念と、治験データに基づく安全性確認について触れられています。) https://soujinkai.or.jp/himawariNaiHifu/replicon-vaccine/
- ワクチン開発・生産体制強化戦略に基づく SCARDA … – 内閣官房(ワクチン開発・生産体制強化戦略(SCARDA)の設立経緯、目的、司令塔機能、研究開発拠点の形成について詳細に記述されています。) https://www.cas.go.jp/jp/seisaku/ful/taisakusuisin/dai17_2025/gijisidai_5.pdf
- ワクチン開発・生産体制強化戦略に基づく ワクチン研究開発等の … – 内閣官房(デュアルユース設備の導入、国内主要企業の取り組み、重点感染症の選定と研究開発ターゲットについて説明されています。) https://www.cas.go.jp/jp/seisaku/ful/taisakusuisin/dai17_2025/gijisidai_4.pdf
- 先進的研究開発戦略センター(SCARDA) – AMED(SCARDAの概要と、平時から感染症有事を見据えた戦略的な研究費配分(ファンディング)の役割について触れられています。) https://www.amed.go.jp/program/list/21/index.html
- 2.1.9 感染症(治療薬・ワクチン) – 科学技術振興機構(JST)(RSウイルスワクチンの開発動向について言及されています。) https://www.jst.go.jp/crds/pdf/2024/FR/CRDS-FY2024-FR-05/CRDS-FY2024-FR-05_20109.pdf
- NEC、経口投与型の個別化がんワクチン「NECVAX-NEO1」の第I相臨床試験における新たなデータをESMO免疫腫瘍学会2025で発表(NECグループによる個別化がんワクチン「NECVAX-NEO1」の第I相臨床試験結果について報告されています。) https://jpn.nec.com/press/202512/20251210_02.html
- ブライトパスが続急伸、BP1212に関する試験データを「IRCI 2025」で発表 – みんかぶ(ブライトパス・バイオによるがん治療薬の治験動向について言及されています。) https://minkabu.jp/news/4266044
- ブライトパス・バイオのご紹介(ブライトパス・バイオのCAR-T細胞療法やCAR-NKT細胞療法の治験について説明されています。) https://daiwair.webcdn.stream.ne.jp/www11/daiwair/qlviewer/pdf/2512134594i2JYlmXo.pdf