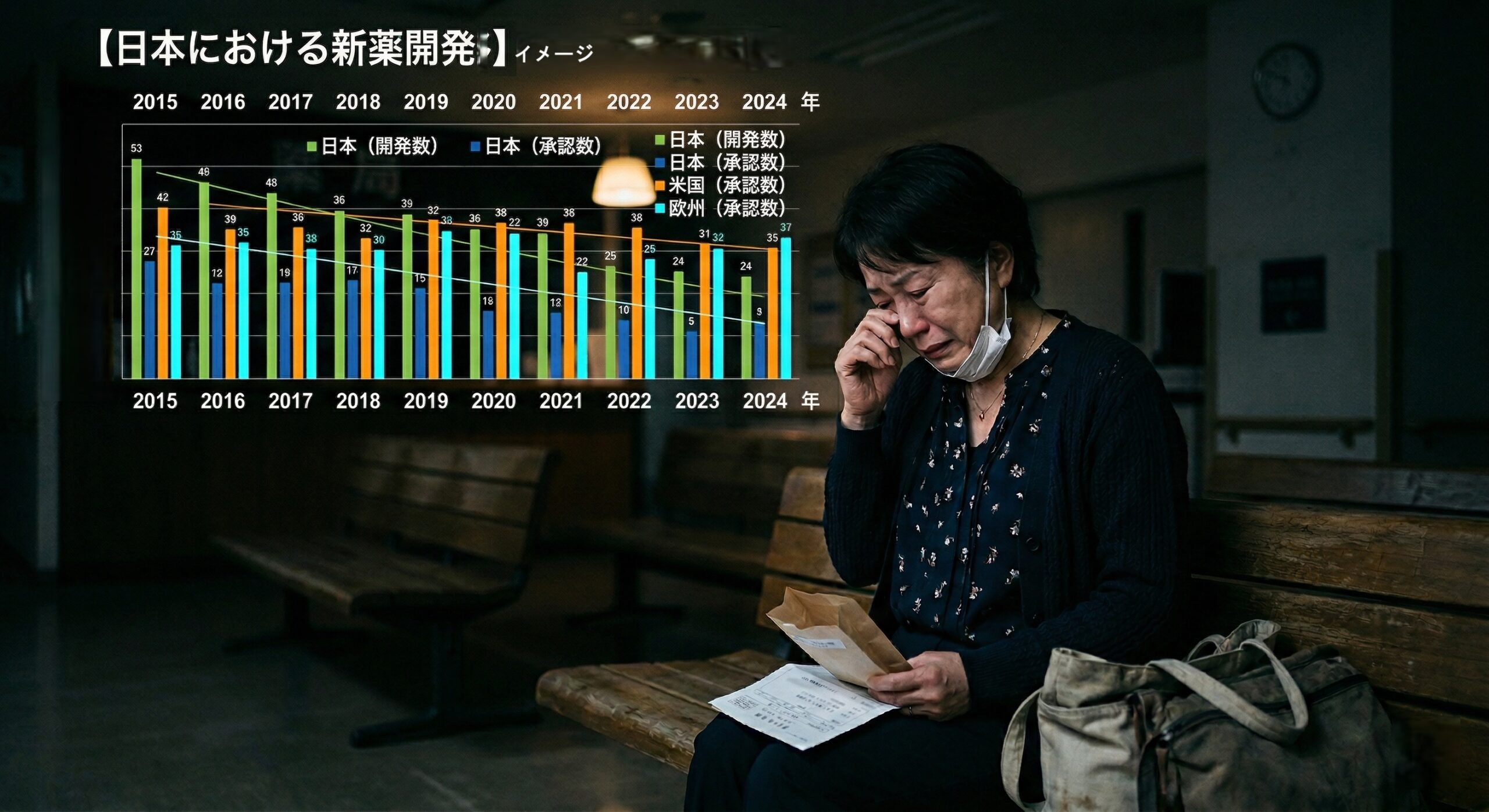
「世界第2位の医薬品消費大国」だった日本が、今や最新の治療薬が届きにくい国になりつつあることをご存じでしょうか?この「ドラッグ・ロス」という静かなる危機は、私たちの健康と未来の医療に深く関わっています。
現在、疾患をお持ちの方向けでは4件の治験・モニター案件が募集中です。疾患がある方・通院のみ・福岡等の案件があります。実施エリアは福岡・関西・関東です。
※2026-04-22時点。最新状況は記事末尾の案件一覧をご確認ください。
かつての医薬品大国・日本が直面する現実:世界市場での地位低下
日本は長年にわたり、米国に次ぐ世界第2位の医薬品市場としての地位を維持し、国民皆保険制度を背景とした安定した需要がグローバル製薬企業にとって大きな魅力でした。しかし、近年の統計データは、その立ち位置が劇的に変化していることを示しています。Hardman & Coの2024年の報告によれば、世界全体の処方薬市場は前年比9.2%の成長を遂げ、総額1兆1,270億ドルに達していますが、その成長の果実を享受しているのは主に米国市場と新興市場です。日本市場の現状を俯瞰すると、2025年の市場規模は11.7兆円と予測され、5年連続の成長を記録しているものの、その成長率は前年比1.7%に留まっており、グローバルな成長ペースからは大きく取り残されています。
世界的なランキングにおいても、日本の相対的な地盤沈下は顕著です。IQVIAなどの調査に基づく2024年の市場規模比較では、米国が7,143億ドルで圧倒的首位を独走し、次いで中国が1,119億ドルで第2位の地位を確固たるものにしています。日本は648億ドルで第3位に位置していますが、ドイツ(647億ドル)との差は極めて僅差であり、経済統計上はもはや第2位の市場とは呼べない状況に陥っています。この衰退を決定づけているのは、単なる市場規模の縮小だけでなく、極めて低い成長率です。主要先進国の中で比較しても、日本の市場年平均成長率はグローバルな成長ペースからは大きく取り残されており、特に2025-2029年の予測複合年間成長率ではマイナス0.8%が見込まれる現実は、投資先としての魅力が著しく低下していることを雄弁に物語っています[3]。
この市場魅力の低下を加速させている要因の一つが、近年の急激な円安と、厳しさを増す薬価抑制政策です。かつては為替が安定しており、薬価も一定の予見性を持っていました。しかし、近年の円安は外資系企業にとって日本での収益を自国通貨ベースで評価した際の目減りを意味し、さらに毎年実施される薬価改定が収益の見通しを著しく不透明にしています。グローバル本社から見れば、1,000億円以上の開発コストと10年以上の歳月を投じて新薬を開発する際、成長が止まり、価格が強制的に下げられ続ける日本市場への優先順位を下げるのは、経済的な合理性に基づいた経営判断と言わざるを得ません。
世界主要国における医薬品市場の成長率と将来予測(2024-2029年)
| 国・地域 | 2024年売上推計(十億ドル) | 2023-24年成長率 | 2025-29年予測複合年間成長率 | 市場の性質とトレンド |
|---|---|---|---|---|
| 米国 | 714.30 | 9.7% | 3-6% | 圧倒的な革新推進力と最大市場 |
| 中国 | 111.90 | 2.5% | 高成長継続 | 第2位市場としての地位を確立、バイオベンチャーの台頭 |
| 日本 | 64.80 | 2.5% | -0.8% | 高齢化による需要増を薬価抑制が打ち消す構造 |
| ドイツ | 64.70 | 7.8% | 安定成長 | 日本を追い越す勢いの欧州最大市場 |
| フランス | 46.50 | 5.3% | 安定成長 | 薬価制度の柔軟性と革新評価の両立 |
| ブラジル | 31.70 | 12.0% | 二桁成長 | 新興市場の急拡大 |
このように、日本市場はもはや「黙っていても新薬が提供される」特権的な地位を失っています。かつては世界市場で大きなシェアを占めていた日本が、2023年には4.4%まで低下している事実は、世界の創薬エコシステムにおいて日本が「周辺的な存在」になりつつある危機を象徴しています。
「ドラッグ・ラグ」から「ドラッグ・ロス」へ:最新治療が届かない深刻な事態

日本における医薬品アクセスの問題は、単なる導入の遅れである「ドラッグ・ラグ」から、そもそも日本での開発が検討すらされない「ドラッグ・ロス」へと、その深刻度を増しています。ドラッグ・ラグについては、医薬品医療機器総合機構(PMDA)の審査スピード向上などの努力により、2022年には16.4カ月まで短縮されており、一定の改善が見られます。しかし、真に危惧すべきは、審査の遅れではなく、企業が日本市場を最初から無視するドラッグ・ロス現象です。
厚生労働省の最新データによれば、2022年末時点で、欧米で承認されているにもかかわらず日本で未承認の新薬は143品目に達しており、そのうち約6割に相当する86品目が、国内での開発にすら着手されていない「ドラッグ・ロス」の状態にあります。この数値は、2016年から2020年にかけて欧米で承認されたNME(新規有効成分含有医薬品)のうち、2022年末時点で日本未承認のものが143品目に上るという事実を裏付けています。かつては「数年遅れで新薬が届く」状況であったものが、現在は「日本にいる限り永遠に新薬が届かない」可能性が現実味を帯びています。
このドラッグ・ロスの背景には、創薬主体の構造変化が深く関与しています。現在のグローバルな新薬開発の主役は、もはや巨大製薬企業(メガファーマ)ではなく、新興バイオ医薬品企業(新興バイオファーマ)へと移行しています。調査によれば、ドラッグ・ロスに陥っている品目の約56%がこれらの新興バイオファーマ由来です[7]。新興バイオファーマはメガファーマのような広範な海外拠点を待たず、限られた資金と人員を最も収益性の高い市場に集中させます。彼らにとって、言語の壁があり、独自な規制要件(日本人を対象とした治験データの要求など)を課し、さらに薬価が抑制される日本市場は、投資対象としての優先順位が極めて低くなるのです。
ドラッグ・ロスの構成要素と特定領域の脆弱性
| カテゴリ | 未着手品目数 | 割合 | 特徴と社会的課題 |
|---|---|---|---|
| 国内開発未着手計 | 86品目 | 100% | 海外承認済みだが、日本での申請計画なし |
| ベンチャー発 | 48品目 | 55.8% | 日本市場の複雑さと低成長を懸念し「日本飛ばし」が発生 |
| 希少疾病用医薬品 | 40品目 | 46.5% | 希少疾患向けで市場規模が小さく、開発コスト回収が困難 |
| 小児用医薬品 | 32品目 | 37.2% | 治験の難易度が高く、経済的インセンティブが不足 |
| 遺伝性疾患 | 21品目 | 24.4% | 特定の遺伝子異常に対する個別化医療、開発ハードル高 |
特に懸念されるのが、小児がんや希少疾患、遺伝性疾患の領域です。ドラッグ・ロス品目の約47%が希少疾病用医薬品指定品目であり、約37%が小児適応を有するものです。これらの疾患を持つ患者にとって、新薬は唯一の希望ですが、市場規模の小ささと開発の難しさから、企業による開発放棄が常態化しています。例えば、2020年から2022年にかけて米国で小児向け適応を取得した抗がん剤40品目のうち、日本で未承認かつ開発の目途が立っていないものが多数存在しており、小児医療における深刻な未充足の医療ニーズを生み出しています。
なぜ日本は選ばれなくなったのか?製薬企業が避ける構造的要因

製薬企業、特にグローバルな投資判断を行う企業視点から見ると、日本市場は「収益の不確実性」と「規制コストの増大」という二重の障壁を抱えています。かつての日本市場の魅力は、国民皆保険の下で「確実に薬が売れ、一定の価格が維持される」という予見性の高さにありましたが、この大前提が近年、崩壊しつつあります。
薬価制度による収益予見性の毀損
製薬企業にとって最大の懸念事項は、毎年のように変更される複雑な薬価算定ルールです。薬価改定が2年に1度から毎年実施に実質的に移行し、さらに「市場拡大再算定」のように、優れた薬として広く普及すればするほど価格が大幅に引き下げられる制度が強化されました。これにより、企業が開発初期段階で見積もった収益予測が容易に覆され、長期的な投資判断を著しく困難にしています。外資系企業各社からは、日本の薬価制度が革新の価値を十分に評価していないという不満が噴出しており、本国のグローバル本社が日本への資源投入を躊躇する決定的な要因となっています。
規制の独自性と手続きの煩雑さ
PMDAの審査自体は世界最速レベルであるものの、治験を開始するまでの「開発ラグ」がいまだに大きな課題として立ちはだかっています。国際共同治験に日本を組み入れる際、日本独自の薬事規制への対応や、日本語での膨大な文書作成が必要となります。特に、日本人での安全性(忍容性)を事前に確認するための第I相試験の実施を求める要件は、迅速なグローバル展開を目指す新興バイオファーマにとって過度な負担と映ります。また、治験審査委員会(IRB)の開催頻度が少なく、審査に時間がかかることや、医療機関ごとに異なる契約手続きの不透明さも、日本を開発拠点から除外する「日本飛ばし」を加速させています。
コストの不透明さと効率性の欠如
開発業務受託機関(CRO)業界の指摘によれば、日本の治験コストは国際標準に比して高額であり、かつ算出根拠が不明瞭であると見なされています。医療機関が請求する臨床試験費用が、国際的な基準(公平な市場価値)と乖離しているケースが多く、さらに日本特有の「生真面目さ」に起因する過剰な品質管理や、ほとんど使用されないデータまでの厳密な確認が、コストを押し上げています。企業は限られた研究開発予算を、より迅速かつ低コストで質の高いデータが得られる韓国や台湾、東南アジア諸国へとシフトさせ始めています。
治験の衰退が私たちの生活に与える影響:医療の質と未来への代償
治験の衰退は、単なる産業上の問題を超え、日本の医療の質、科学技術の競争力、そして国民の生命そのものを脅かす静かな危機です。この「治験の空洞化」が日本社会に及ぼす影響は、多層的かつ不可逆的な性質を帯びています。
患者の治療選択肢の喪失と医療格差の拡大
最も直接的かつ悲劇的な影響は、日本の患者が世界標準の最新治療を受けられなくなることです。がんや希少疾患の治療において、海外ではすでに標準薬として使用されている新薬が日本に存在しないという事態は、日本の医療の質が世界水準から転落することを意味します。患者団体からは、審査の優先化や製薬企業への開発要請を求める切実な声が上がっていますが、ドラッグ・ロスが解消されない限り、日本は「特定の病気においては治療の選択肢がない国」へと成り下がってしまうでしょう。これは、日本に居住していること自体がリスクとなる、医療アクセスの不平等という新たな社会課題を生み出します。
医療現場の知見停滞と科学的空洞化
治験は、医師や研究者が最新の薬剤や治療プロトコールに触れる貴重な機会でもあります。日本が国際共同治験から除外され続けると、日本の医師は最新の治療法に関する臨床知見を蓄積できなくなります。最先端の治療法を知らない医師は、国際的な医学界での主導権を失い、日本の医学研究全体のレベルが低下します。これは、若く優秀な医師や研究者が、最新の臨床環境を求めて米国や欧州へと流出する「頭脳流出」を招き、国内のライフサイエンス基盤をさらに弱体化させるでしょう。
経済的損失と創薬エコシステムの崩壊
治験に関連する投資は、医療機関や開発業務受託機関、周辺産業に多大な経済的インパクトをもたらします。日本が治験から選ばれなくなることは、これらの経済的リターンが海外へ流出することを意味します。また、国内の創薬スタートアップが画期的なシーズを開発しても、出口としての日本市場に魅力がなければ、最初から海外企業に権利を売却し、日本国内での臨床開発を行わない可能性が高まります。これにより、日本の税金や知恵で生まれた革新が日本国内の患者に還元されず、経済的利益も海外に吸収されるという、創薬エコシステムの崩壊を招きます。
アジアにおける国際共同治験の参加状況比較(2023年時点)
| 国・地域 | 累積参加数順位 (2000-23) | 新興バイオファーマ主導治験の参加数 | 治験環境の強み | 日本との相対的優位性 |
|---|---|---|---|---|
| 韓国 | 上位維持 | 514 | 国を挙げたインフラ整備、迅速な手続き | 新興バイオファーマ主導で日本の約2.4倍の実施数 |
| 日本 | 19位 (上昇傾向) | 214 | 高い症例の質、PMDAの審査速度 | 手続きの煩雑さと高コストが課題 |
| 台湾 | 安定 | 360 | 効率的な臨床試験ネットワーク | 日本を上回る新興バイオファーマ誘致実績 |
| 中国 | 急上昇 | 253 | 圧倒的な患者数と市場の将来性 [13] | 市場規模を背景とした強い引き合い [13] |
特に、韓国の躍進は日本の失策を浮き彫りにしています。韓国は政府が多数の臨床試験センターに多額の予算を投じ、治験手続きの迅速化とコストの透明化を徹底しました。その結果、特にスピードとコストを重視する新興バイオファーマ主導の治験において、日本は韓国の半分以下の実績しか残せていません。この差は、将来の医薬品アクセスの差に直結します。
日本の医療再生への道筋:官民一体の改革と治験の新たな役割
日本の医薬品市場の危機的状況を打破すべく、厚生労働省や関係各所は、従来の延長線上ではない抜本的な改革に乗り出しています。2024年度は、その再生に向けた重要な転換点と位置づけられます。
厚生労働省による「ドラッグ・ロス解消に向けた新規ルート」
これまでの未承認薬対策は、学会や患者団体からの要望を受けて検討する受動的なものでしたが、令和6年度からは国が能動的に情報を整理し、開発を加速させる「新規ルート」が始動しました。
- 能動的情報の整理: 欧米で承認され日本で未開発の86品目に対し、国が自ら学会へのニーズ調査や市場性調査を実施し、開発の優先順位(グループA〜D)を決定します。
- 開発の加速化措置: 優先度の高い品目(グループAの14品目など)について、企業への開発要請を迅速化し、開発を希望する企業を公募します。
- アカデミア支援の強化: 市場性の欠如などで企業が着手しにくい場合、日本医療研究開発機構(AMED)による支援を通じ、学術機関主導での薬事承認申請用データ取得を支援します。
薬価制度の抜本的見直し(2024年度改革)
市場の魅力を高めるため、薬価制度にも「革新への報奨」という観点が強化されました。特に、ドラッグ・ロス解消へのインセンティブとして以下の措置が導入されています。
- 「新薬創出加算」の改善: 革新的な新薬について、特許期間中は薬価を実質的に維持する仕組みを強化し、投資回収の予見性を向上させました。
- 「迅速導入加算」の拡充: 日本で世界に先駆けて、あるいは世界との差を最小限にして導入する品目に対し、高い加算を付与する仕組みを整えました。
- 小児・希少疾患薬の評価: 開発コストがかさむ一方で市場が限定的な分野に対し、高い加算率や維持措置を講じ、新興バイオファーマの参入障壁を下げています。
治験プロセスの効率化と開発業務受託機関の取り組み
治験環境の改善に向け、日本開発業務受託機関協会などは「日本の治験は遅い・高い」という誤った、あるいは旧来の認識を払拭するための情報発信を強化しています。具体的には、国際標準コスト(公平な市場価値)の導入による透明性の向上、治験審査委員会の共通化やオンライン化による審査スピードの短縮、さらに分散型治験の推進による被験者登録の加速などが進められています。
日本が再び魅力的な医薬品市場として返り咲き、国民に最新の医療を提供し続けるためには、一時的な補助金や一部の加算といった断片的な処置では不十分です。求められているのは、日本の医療・薬事システム全体をグローバルな創薬エコシステムに「再接続」することです。
まず、薬価制度においては、単なる予算管理の道具としての価格引き下げから、革新を呼び込むための「投資の引き金」としての役割を再認識する必要があります。市場の予見性を高め、優れた新薬が適切に評価される環境がなければ、外資系企業の日本離れは止まらないでしょう。次に、治験インフラの徹底的な効率化です。韓国や台湾に後塵を拝している現状を直視し、行政手続きのデジタル化、言語障壁の撤廃、そして多地域共同治験への初期段階からの参画を制度的に促すべきです。
ドラッグ・ロスの問題は、日本の医療制度が直面している「静かなる危機」です。最新の治療薬が届かない現状は、国民の健康を損なうだけでなく、日本の科学技術と産業競争力を根本から蝕みます。しかし、2024年以降の政策転換は、この危機に対する覚醒の兆しでもあります。行政、産業界、そして学術界が一体となり、日本の患者が「世界最高の医療」を等しく享受できる体制を再構築できるかどうかが、今後の10年の日本の姿を決定づけるでしょう。日本市場が再び選ばれる市場となることは、単なる産業の成功を意味するのではなく、日本の国民一人ひとりの命を守り抜くという、国家の根幹に関わる使命です。
治験ネットについて
「時間を、価値に変える。未来を、健康でつなぐ。」
治験ネットは、治験への参加を「時間の投資」と捉え、納得できる情報提供を大切にしています。ワクチン・生活習慣病・美容など幅広い分野の募集情報を掲載中。会員登録(無料)で、あなたの条件に合った案件を確認できます。
→ 会員登録ページへ
参考・出典
- 2024 PHARMA STATISTICS – Hardman & Co https://hardmanandco.com/wp-content/uploads/2025/04/250403-Hardman-Co-Insight-2024-Pharma-Statistics.pdf
- Japan Pharma Market Up 1.7% in 2025, 5th Straight Year of Growth: IQVIA https://pj.jiho.jp/article/254831
- Pharmaceutical Market Size by Country 2026 – World Population Review https://worldpopulationreview.com/country-rankings/pharmaceutical-market-size-by-country
- The Global Use of Medicines 2025: Outlook to 2029 – IQVIA https://www.iqvia.com/-/media/iqvia/pdfs/events/presentation_global-meds-webinar_public.pdf
- なぜ最新薬は日本に届かない?外資製薬から見た日本の壁|ヘルス … https://note.com/realworld/n/n4a75ebdb008c
- CRO業界としてのドラッグラグ/ロスの問題と取り組み – 製薬協 https://www.jpma.or.jp/information/evaluation/symposium/bbh7c90000001esq-att/2023_11_17_03.pdf
- 企業視点によるドラッグラグ・ドラッグロスの要因分析および解消 … https://www.jstage.jst.go.jp/article/rsmp/16/1/16_79/_article/-char/ja
- The Pharmaceutical Industry in Figures – EFPIA https://www.efpia.eu/media/uj0popel/the-pharmaceutical-industry-in-figures-2025.pdf
- ドラッグ・ロスの現状及び対策 – 国立国会図書館デジタルコレクション https://dl.ndl.go.jp/view/prepareDownload?itemId=info:ndljp/pid/14118371
- ドラッグラグとは?日本の医薬品承認の遅れがもたらす影響と対策 – Salesforce https://www.salesforce.com/jp/blog/jp-drag-rug/
- ドラッグロス解消に向けた取組(令和6年度~)検討状況 – 厚生労働省 https://www.mhlw.go.jp/content/11121000/001568902.pdf
- ドラッグ・ロスを招く日本の薬価制度への提言 ~海外企業にとって … https://waseda.repo.nii.ac.jp/record/2006063/files/57233029_202503.pdf
- 近年における国際共同治験の動向調査 https://www.jpma.or.jp/opir/news/073/j5cv6u0000000727-att/73_2.pdf
疾患をお持ちの方向けの募集中案件
※案件情報は2026-04-22時点のものです。最新の募集状況は各案件ページでご確認ください。
疾患をお持ちの方向けの新着案件情報
他にも4件以上の案件が募集中です。無料会員登録すると、新着案件をメールでお知らせします。
無料会員登録はこちら※登録は約1分で完了します。治験への参加義務はありません。